Semana 11-Martes
Semana11
SESIÓN
31
|
Unidad 2. Oxígeno, sustancia activa del aire
Compuestos del oxígeno y clasificación de los elementos
|
contenido temático
|
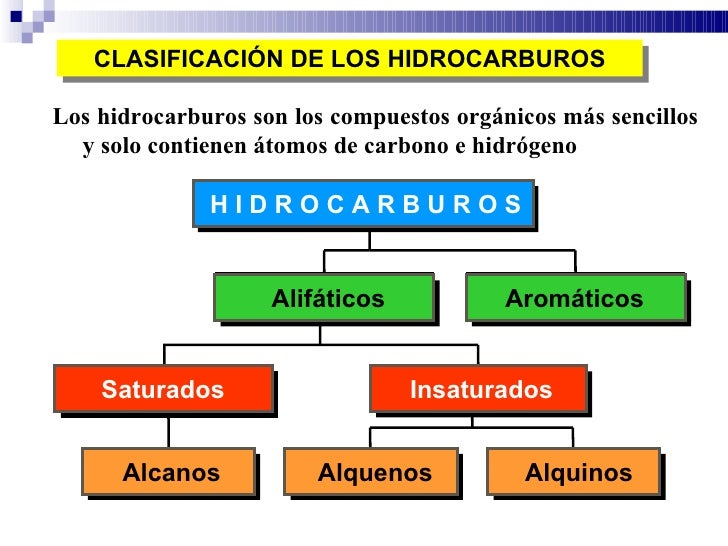
Hidrocarburos saturados e insaturados(8C)
Nomenclatura
|
Aprendizajes esperados del grupo
|
Conceptuales
3. Reconoce la importancia de la ciencia y el uso de argumentos basados en evidencias para discutir y resolver problemas de importancia económica, social y ambiental, al estudiar el debate en torno del efecto de invernadero y el cambio climático. (N2)
Procedimentales
Actitudinales
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Materiales generales
|
Computo:
De proyección:
Programas:
Didáctico:
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Desarrollo del
Proceso
|
Introducción.
Presentación del Profesor y del alumno, el programa del curso, comentar el papel, así como la dinámica del curso y factores a considerar en la evaluación.
FASE DE APERTURA
FASE DE DESARROLLO
Los alumnos desarrollan las actividades de acuerdo a las indicaciones del Profesor por equipo completar y balancear las ecuaciones siguientes:
Ejemplo:
• Auxilia a los estudiantes para identificar la información que está contenida en la tabla periódica, por ejemplo: masa atómica, número de oxidación, número atómico, etcétera. Mediante ejercicios promueve el uso de la tabla periódica para caracterizar elementos y compuestos por su masa atómica, masa fórmula y masa molecular. (A5) • Con base en la organización de la tabla periódica moderna, presenta a los estudiantes las propiedades como energía de ionización y electronegatividad para explicar las propiedades de los metales y no metales y la abundancia de los primeros. (A5)
• Realiza una experiencia de cátedra en la que muestra la reactividad de Fe, Na, K, y Mg con agua para relacionar la actividad química de éstos y su posición en la tabla periódica. (A5)
Esta actividad permitirá a los alumnos, tener un panorama de los temas que se desarrollaran durante el curso. (Que, cuando, como y donde)
FASE DE CIERRE
Al final de las presentaciones, se lleva a cabo una discusión extensa, en la clase, de lo que se aprendió y aclaración de dudas por parte del Profesor.
Actividad Extra clase:
Los alumnos llevaran la información para procesarla en el Centro de Computo del Plantel, su casa los que tengan computadora e internet o cibercafé e indagaran los temas de la siguiente sesión, de acuerdo al cronograma.
Se les sugiere que abran un Blog para Química 1; en la cual publicaran su información, se les solicitara que los equipos formados, se comuniquen vía Gmail u otro programa para comentar y analizar los resultados y presentarla al Profesor en la siguiente clase.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Evaluación
|
Informe de la actividad en un documento electrónico.
Contenido:
Resumen de la Actividad.
|


Comentarios
Publicar un comentario